Traducido con IA
El 27 de noviembre de 2025, la Comisión Europea anunció la plena funcionalidad de cuatro de los seis módulos de EUDAMED a través de la Decisión (UE) 2025/2371, publicada en el Diario Oficial.
Esto inicia un periodo de transición de 6 meses, estableciendo la obligatoriedad del uso de los primeros cuatro módulos a partir del 28 de mayo de 2026. Los operadores económicos que aún no hayan utilizado los módulos de forma voluntaria deben actuar lo antes posible.
Los 4 módulos funcionales de EUDAMED
Los módulos declarados plenamente operativos y obligatorios a partir del 28 de mayo de 2026 son:
- Módulo «Actor Registration» ACT (Registro de Actores)
Tiene como objetivo el registro obligatorio de los operadores económicos, es decir, fabricantes (incluidos los fabricantes de sistemas y kits procedimentales), representantes autorizados e importadores, con el fin de obtener el Single Registration Number (SRN). Este registro es un requisito previo necesario para todas las operaciones posteriores en los módulos de EUDAMED, según lo previsto en los artículos 31 del MDR (UE) 2017/745 y 28 del IVDR (UE) 2017/746. - Módulo «UDI/Devices Registration» UDI/DEV (Registro de UDI y Productos)
Gestiona los identificadores UDI (UDI-DI/UDI-PI) a través de una base de datos central para los productos MDR/IVDR. Recopila información detallada sobre los productos, incluyendo la clase de riesgo, el UDI básico y los datos relativos al acondicionamiento y unidades de venta. Para los productos legacy (MDD/IVDD) y regulados, así como para los productos a medida o aquellos cuyas unidades individuales ya no se introduzcan en el mercado tras la obligatoriedad del módulo, el registro solo se realizará en caso de incidentes graves, acciones correctivas de seguridad (FSCA) o necesidades de vigilancia, utilizando identificadores específicos EUDAMED DI/ID en lugar del UDI estándar. - Módulo «Notified Bodies and Certificates» NB/CRF (Organismos Notificados y Certificados)
Permite a los Organismos Notificados (ON) registrar y gestionar los certificados emitidos para productos conformes con el MDR e IVDR. Asimismo, recopila los Resúmenes sobre Seguridad y Funcionamiento Clínico (SSCP), transmitidos directamente por los Organismos Notificados para los productos de mayor riesgo. - Módulo «Market Surveillance» MSU (Vigilancia del Mercado)
Reserva el acceso a las Autoridades Competentes para la gestión de las actividades de vigilancia del mercado en la fase poscomercialización, incluidas las inspecciones y la gestión de las no conformidades.
Prioridades para los fabricantes
Con un periodo de transición de solo seis meses, los fabricantes deben centrarse en los módulos ACT y UDI/DEV, que son de su directa responsabilidad:
- Prioridad 1: obtener el Single Registration Number (SRN).
Acción fundamental: sin el SRN es imposible proceder con el resto de los registros. - Prioridad 2: preparar los datos UDI para el módulo UDI/DEV.
Revisar y organizar los detalles de los códigos UDI para evitar bloqueos en la comercialización de los productos.
Plazos y excepciones para los 4 módulos
La fecha oficial de inicio de la obligatoriedad de uso de los 4 módulos es el 28 de mayo de 2026; se recomienda cumplir con este plazo de forma prioritaria en todos los casos. No obstante, el Reglamento (UE) 2024/1860 prevé algunas excepciones temporales específicas:
Fabricantes (Módulo UDI/DEV)
- Para los productos conformes a MDR e IVDR introducidos en el mercado antes del 28 de mayo de 2026, los fabricantes cuentan con una prórroga de 6 meses extra (hasta el 28 de noviembre de 2026) para el registro en el módulo UDI/DEV.
- Excepción: la prórroga no se aplica si los productos están involucrados en actividades de vigilancia (PMSV, MIR, FSCA o informes de tendencias), que requieren un registro inmediato.
Organismos Notificados (Módulo NB/CRF)
- Los Organismos Notificados tienen una prórroga de 12 meses extra (hasta el 28 de mayo de 2027) para registrar en el módulo NB/CRF los certificados emitidos y los Master SSCP (para clases IIb/III) relativos a los productos introducidos en el mercado antes del 28 de mayo de 2026.
- Excepción: la prórroga queda anulada en caso de acciones de vigilancia (incidentes graves, PSUR, FSCA o notificaciones obligatorias).
Tabla resumen de plazos
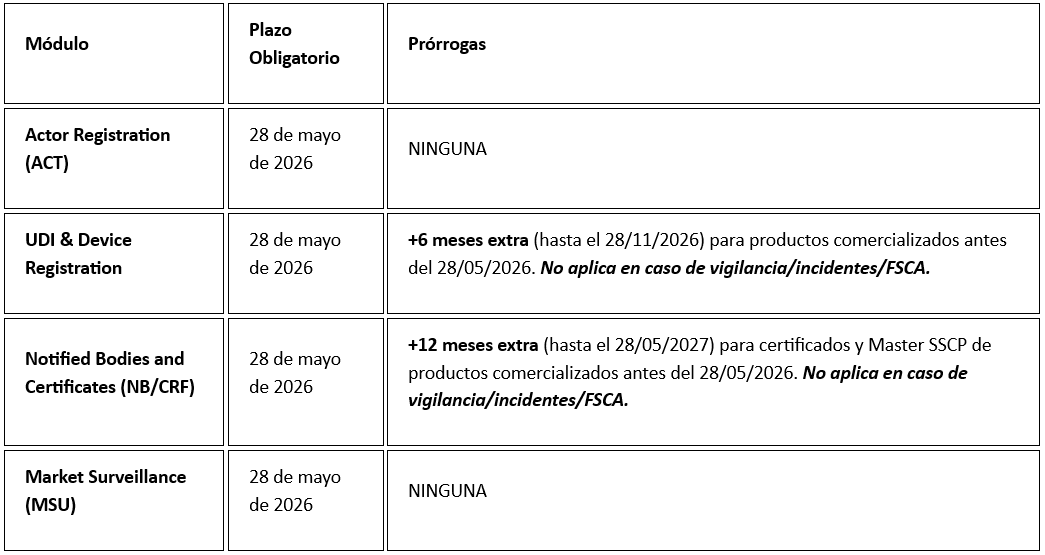
La obligatoriedad de los módulos EUDAMED no es una meta, sino el punto de partida para una gestión centralizada y transparente del producto durante todo su ciclo de vida.
No hay más tiempo que perder. Es fundamental finalizar lo antes posible el registro en el módulo ACTOR y en el módulo UDI/DEV para evitar interrupciones operativas y riesgos de no conformidad.
Para consultoría estratégico-regulatoria, formación y soporte directo en el uso de los módulos EUDAMED, los expertos de Thema están a su lado. Contactar con: sales@complifegroup.com
FUENTES:



