EUDAMED es la base de datos desarrollada por la Comisión Europea para centralizar y hacer fácilmente accesible la información sobre productos sanitarios y productos para diagnóstico in vitro (IVD), tal como exigen los Reglamentos MDR (UE) 2017/745 e IVDR (UE) 2017/746.
Tras años de aplazamiento, EUDAMED por fin está tomando forma, y con ella llegan nuevos plazos y obligaciones para los fabricantes de productos sanitarios. El Reglamento (UE) 2024/1860 actualizó la hoja de ruta para el despliegue gradual de EUDAMED y la finalización del sistema se estima para 2027.
La plataforma EUDAMED consta de seis módulos interconectados. Actualmente, hay tres módulos activos y utilizables de forma voluntaria (ACTOR, UDI/Dispositivos, Organismos Notificados y Certificados) para ofrecer a los fabricantes la oportunidad de adaptarse con antelación y reducir el riesgo de futuros retrasos.
También hay que tener en cuenta que en 2026, se espera que los primeros módulos de EUDAMED sean obligatorios: el módulo «Actor» (ACT) y el módulo «UDI/Dispositivo» (UDI/DEV), el Módulo de Organismos Notificados y Certificados (NB/CRF) y el Módulo de Vigilancia y Supervisión Postcomercialización (VGL). Véase la actualización del 27 de noviembre de 2025.
¿Cuáles son los cambios y las implicaciones para los agentes económicos en relación con cada módulo?
Analizaremos estos aspectos a lo largo del artículo.
Aplicación gradual de EUDAMED: ¿qué cambia?
El artículo 34 del MDR, modificado por el Reglamento 2024/1860, estipula que los módulos EUDAMED pasan a ser obligatorios seis meses después de la publicación del anuncio de plena funcionalidad en el Diario Oficial de la Unión Europea (DOUE). Una auditoría independiente verificará la conformidad del módulo, tras lo cual se publicará el anuncio oficial de activación.
No obstante, existen plazos adicionales para registrar determinados dispositivos y sus certificados en EUDAMED. En particular, para los productos heredados y los que cumplen los reglamentos MDR e IVDR que siguen comercializándose después de la fecha de uso obligatorio de los formularios de registro y certificado de los productos, el Reglamento (UE) 2024/1860 introdujo disposiciones adicionales
- 6 meses de prórroga para los fabricantes.
- 12 meses de plazo adicional para los organismos notificados que, para estos productos, solo tendrán que registrar la última versión del certificado correspondiente y, en su caso, la decisión pertinente.
Los plazos adicionales previstos para el registro de los productos no se aplican si, una vez que el uso del módulo de vigilancia también se ha hecho obligatorio, los productos están sujetos a:
- PSUR – Periodic Safety Update Report (Informe periódico de actualización en materia de seguridad)
- Accidente grave
- Medidas correctoras en materia de seguridad
- Informe de tendencias
En estos casos, el registro de los dispositivos es una acción necesaria y previa a la posibilidad de utilizar las funcionalidades del módulo de vigilancia.
En otras palabras, si en el periodo de tiempo adicional el módulo de vigilancia también pasa a ser obligatorio, entonces el fabricante no puede esperar los 6 o 12 meses para registrar los dispositivos: debe registrarlos ahora, antes de que se pueda utilizar el módulo de vigilancia.
La directriz de 21 de noviembre de 2024 «Despliegue gradual de EUDAMED – Preguntas y respuestas sobre aspectos prácticos relacionados con la aplicación del Reglamento (UE) 2024/1860» aportó importantes aclaraciones.
Módulos EUDAMED: características y calendario
- Módulo de registro de actores (ACT)
Permite a los fabricantes (incluidos los de sistemas y kit de procedimiento), agentes e importadores registrarse para obtener un número de registro único (SRN). Las Autoridades Competentes validan los datos de los operadores económicos antes de asignarles el número SRN.
- Activo con carácter voluntario a partir del 1 de diciembre de 2020. Véase la actualización del 27 de noviembre de 2025.
- Obligatorio seis meses después de la publicación del anuncio oficial en el DOUE. La obligación está prevista para 2026.
- El registro en ACT también es necesario para los operadores con dispositivos heredados en el mercado.
- Módulo de registro de UDI/dispositivos (UDI/DEV)
Gestiona el registro y la gestión de los identificadores UDI de los Dispositivos Médicos.
- Activo con carácter voluntario a partir del 4 de octubre de 2021.
- Los fabricantes pueden seguir registrando productos en las bases de datos nacionales, pero el formulario UDI/DEV, ya disponible de forma voluntaria, las sustituirá por completo seis meses después de la publicación del anuncio en el Diario Oficial. La obligación está prevista para 2026. Véase la actualización del 27 de noviembre de 2025.
- Para los productos comercializados después de la fecha en que el módulo pase a ser obligatorio: registro obligatorio antes de la primera comercialización.
- Para los productos comercializados antes de la fecha en que el formulario pase a ser obligatorio: registro en un plazo de doce meses a partir de la publicación del anuncio en el Diario Oficial.
- Los productos heredados y los productos regulados cuyas unidades individuales (de venta) ya no se comercialicen a partir de la fecha en que el formulario UDI/DEV sea obligatorio, solo deberán registrarse en el formulario UDI/DEV cuando se trate de accidentes o acciones correctivas de seguridad. Lo mismo se aplica a los dispositivos hechos a medida.
Ejemplo: Un producto comercializado entre mayo de 2021 y noviembre de 2025 no tendrá que registrarse en EUDAMED si el módulo UDI/DEV pasa a ser obligatorio en 2026. Sin embargo, si el Módulo de Vigilancia y Vigilancia Postcomercialización (VGL) pasa a ser obligatorio en julio de 2026 y el producto está sujeto a vigilancia en septiembre de 2026, será necesario registrarlo.
Si una acción de vigilancia se refiere a un producto sanitario heredado que no está registrado como «mismo producto» que ya cumple la normativa, excepcionalmente tendrá que registrarse en el módulo UDI/DEV para permitir la notificación en el módulo de Vigilancia y Vigilancia Postcomercialización (VGL).
La regla general sigue siendo: los dispositivos heredados no requieren registro si «el mismo dispositivo» ya está registrado.
Es importante tener en cuenta que los dispositivos heredados no están sujetos a las obligaciones UDI en virtud de MDR. No obstante, para permitir su registro en EUDAMED, se asignarán identificadores únicos específicos, denominados DI EUDAMED e ID EUDAMED, que sustituirán al UDI-DI básico y al UDI-DI.
- Formulario para organismos notificados y certificados (ON/CRF)
Permite a los organismos notificados (ON) registrar y gestionar los certificados expedidos para los productos que cumplen los requisitos de MDR e IVDR. Además, los ON deben cargar el Resumen de Seguridad y Rendimiento Clínico (SSCP) para los dispositivos de mayor riesgo.
- Activo con carácter voluntario a partir del 4 de octubre de 2021, a excepción de la funcionalidad del mecanismo de examen y del Procedimiento de Consulta de Evaluación Clínica (CECP). Véase la actualización del 27 de noviembre de 2025.
- Certificados expedidos después de la fecha obligatoria: inscripción inmediata.
- Certificados expedidos antes de la obligatoriedad: registro en un plazo de 18 meses a partir de la publicación en el Diario Oficial, solo si están asociados a productos registrados en el formulario UDI/DEV.
- Módulo de Vigilancia y Vigilancia Postcomercialización (VGL)
Gestiona los informes de eventos adversos, incidentes y Acciones Correctivas de Seguridad de Campo (FSCA).
- Fabricantes y agentes: obligación de notificar efectos adversos y FSCA.
- Las autoridades competentes supervisan y evalúan las medidas correctoras.
- No es operativo; será obligatorio seis meses después de la publicación del anuncio de plena funcionalidad.
- Módulo de investigaciones clínicas y estudios de rendimiento (CIP)
Permite el registro y seguimiento de estudios clínicos sobre productos sanitarios y de diagnóstico in vitro.
- Autoridades competentes: aprobar y supervisar los estudios.
- No es operativo; será obligatorio seis meses después de la publicación del anuncio de plena funcionalidad.
- Unidad de Vigilancia del Mercado (MSU)
Reservada a las Autoridades Competentes para gestionar las inspecciones y las no conformidades.
- Acceso limitado a las Autoridades y, en algunos casos, a los Organismos Notificados.
- No es operativo; será obligatorio seis meses después de la publicación del anuncio oficial de plena funcionalidad. Véase la actualización del 27 de noviembre de 2025.
Cuadro recapitulativo
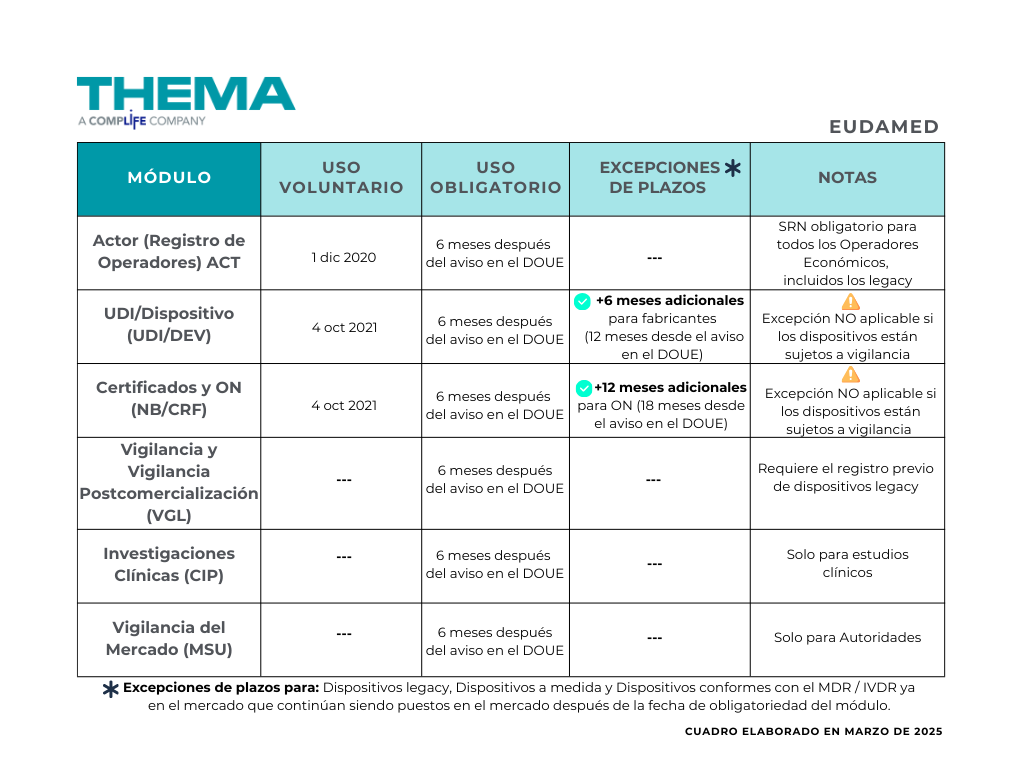
Cómo prepararse para EUDAMED
Para los fabricantes, la aplicación gradual de EUDAMED representa un reto importante, pero también una oportunidad para adaptarse a un sistema europeo más eficaz y centralizado de gestión de la información sobre productos sanitarios. Es esencial que los fabricantes adopten una estrategia de adaptación a EUDAMED, empezando por el uso de los módulos disponibles de forma voluntaria y manteniéndose al día de la evolución de la base de datos, con vistas a la adopción obligatoria de los módulos.
Con la obligatoriedad del formulario ACTOR y UDI prevista para 2026, no hay tiempo que perder. Es esencial tomar medidas lo antes posible. Véase la actualización del 27 de noviembre de 2025.
>>> Thema sigue la evolución de EUDAMED y está al lado de los fabricantes y otros operadores económicos para consultoría estratégico-normativa y para actividades de apoyo en el uso de módulos EUDAMED ya activos.
Actualización del 27 de noviembre de 2025
El 27 de noviembre de 2025, la Comisión Europea anunció la plena funcionalidad de cuatro de los seis módulos de EUDAMED mediante la Decisión (UE) 2025/2371 publicada en el Diario Oficial. Véase el artículo completo.
FUENTES Y RECURSOS ÚTILES
- “Gradual roll out of EUDAMED – Q&As on practical aspects related to the implementation of Regulation (EU) 2024/1860”
- MDCG 2021-13 rev.1 Questions and answers.
- https://health.ec.europa.eu/medical-devices-eudamed/overview_en
- EUDAMED user guide Legacy Devices
- https://www.salute.gov.it/portale/dispositiviMedici/dettaglioContenutiDispositiviMedici.jsp?lingua=italiano&id=5610&area=dispositivi-medici&menu=eudamed
- https://health.ec.europa.eu/document/download/fb6f6ec5-d0eb-4edc-b168-8e74cfa0c89e_en?filename=md_eudamed_20250521_co1
19/03/2025



