Il codice UDI deve essere applicato in punti specifici per garantire la massima accessibilità e leggibilità:
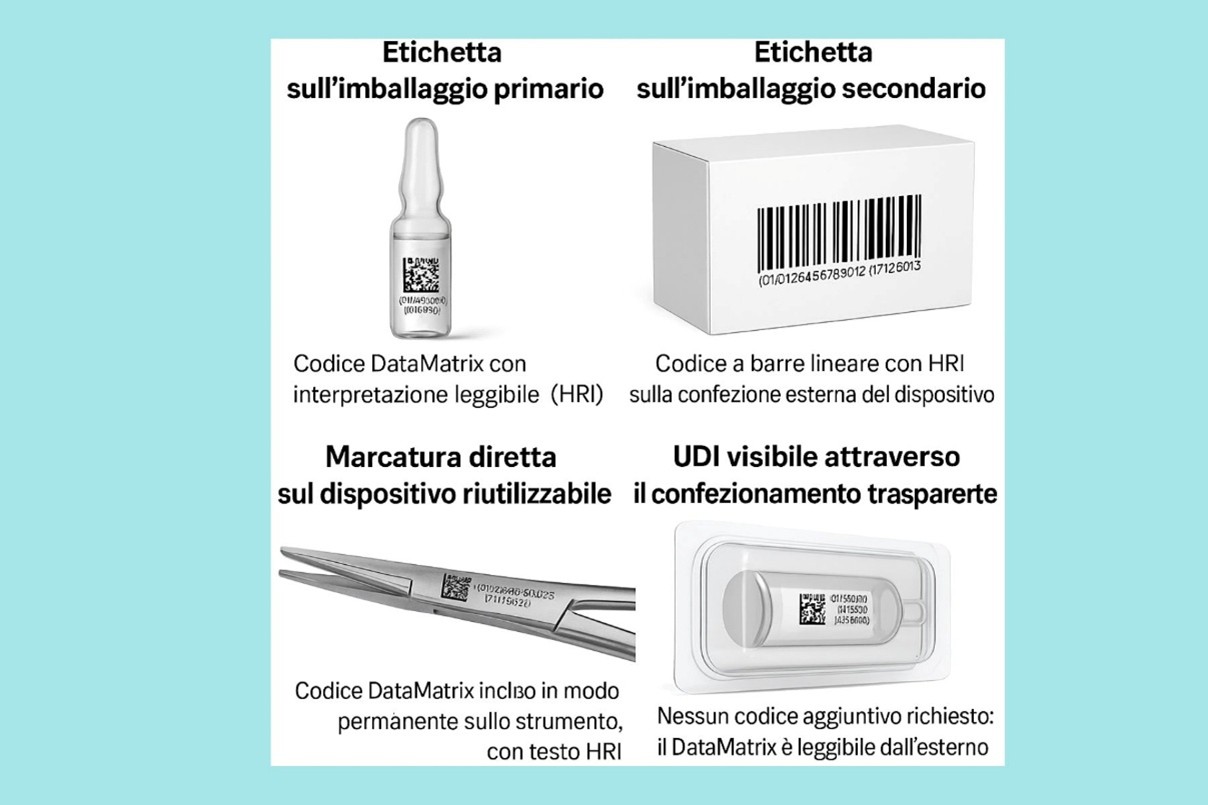
- Su tutti i livelli di confezionamento: sull’etichetta dell’imballaggio primario (il primo involucro che entra direttamente a contatto con il dispositivo o il prodotto) e sull’imballaggio secondario (l’involucro esterno che contiene uno o più imballaggi primari).
- Direttamente sul dispositivo stesso (marcatura UDI permanente): se tecnicamente fattibile e se il dispositivo è destinato al riutilizzo. In questo caso, spesso si usa un Codice DataMatrix inciso in modo permanente.
Per quanto riguarda l’imballaggio terziario, tipicamente utilizzato per la spedizione, non è previsto l’obbligo di riportare l’UDI del singolo dispositivo, sebbene possa ospitare codici UDI di aggregazione.
L’UDI deve apparire in due formati complementari:
- AIDC (Automatic Identification and Data Capture): formato leggibile da scanner e sistemi automatizzati (es. DataMatrix, codice a barre lineare).
- HRI (Human Readable Interpretation): formato testuale chiaro leggibile dall’uomo.
Eccezioni e regole aggiuntive:
- Spazio limitato: se lo spazio sull’etichetta è troppo ridotto, è sufficiente riportare solo il formato AIDC.
- Dispositivi per uso esterno a strutture sanitarie (es. assistenza domiciliare): per questi dispositivi, la parte leggibile dall’uomo (HRI) è sempre obbligatoria, anche qualora ciò impedisse di includere il formato scansionabile (AIDC).
- Gerarchia di confezionamento: se l’UDI non può essere posto sull’imballaggio dell’unità d’uso per mancanza di spazio, può essere posizionato sul livello di confezionamento immediatamente superiore, che deve avere un proprio UDI unico.
- Dispositivi monouso di classe I e IIa (Dispositivi Medici) e di classe A e B (IVD) confezionati singolarmente: per questi dispositivi, il supporto UDI non è richiesto sull’imballaggio dell’unità individuale, a condizione che il supporto UDI sia collocato sul livello superiore di confezionamento immediatamente successivo e che possa essere facilmente identificato e recuperato dall’utilizzatore.
- Dispositivi esclusivamente per la vendita al dettaglio: l’UDI in formato AIDC non è obbligatorio se è sostituito da un codice a barre EAN/UPC standard.
- Trasparenza dell’imballaggio: se l’UDI è già chiaramente leggibile o scansionabile attraverso il confezionamento, non è necessario apporre un supporto UDI aggiuntivo sull’imballaggio stesso.
Per ulteriori dettagli, consultare la Sezione 4 dell’Allegato VI Parte C dei Regolamenti MDR e IVDR.
Esempi di apposizione UDI su Dispositivi Medici