Il sistema di sorveglianza post-market (PMS) serve a “raccogliere, registrare e analizzare attivamente e sistematicamente i pertinenti dati sulla qualità, le prestazioni e la sicurezza di un dispositivo durante l’intero periodo di validità, a trarre le necessarie conclusioni e a determinare, attuare e monitorare le eventuali azioni preventive e correttive” (Rif. Art. 83 dell’MDR).
La necessità di tale sistema sorge immediatamente dopo la commercializzazione del dispositivo. Il sistema PMS serve non solo per soddisfare i requisiti normativi, ma anche per migliorare la gestione dei rischi e migliorare la qualità di un dispositivo medico. Il sistema PMS serve per identificare opportunamente problemi nel design e/o nell’utilizzo del dispositivo e per caratterizzare accuratamente il comportamento di tale dispositivo nelle normali condizioni d’uso e i risultati clinici ottenuti.
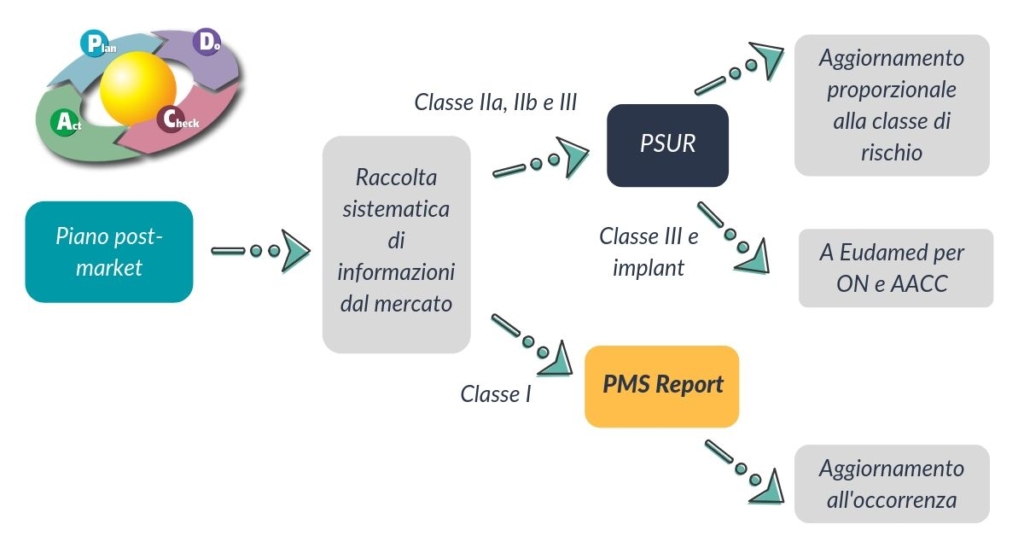
La vigilanza è anche essa parte del sistema PMS. Parte “viva” del sistema PMS e elementi fondamentali dell’ SGQ sono anche il follow-up clinico post-market (PMCF, per i Dispositivi Medici) e il follow-up delle prestazioni post-market (PMPF, per gli IVD). Tali processi continui, che fanno parte della valutazione clinica/delle prestazioni, sono rivolti a colmare il gap tra le evidenze raccolte durante la fase pre-market e i dati PMS raccolti sul dispositivo già in uso.
Domande? Chiedi maggiori informazioni ai nostri specialisti
CONTATTACI




